Атрезия пищевода
Последняя редакция: 14.03.2024

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
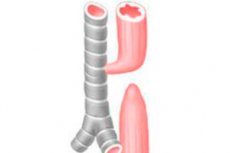
Атрезия пищевода (АП) - врожденный порок развития, при котором пищевод слепо заканчивается на расстоянии примерно 8-12 см от входа в ротовую полость.
Врождённый трахеально-пищеводный свищ без атрезии - патологический канал, выстланный грануляционной тканью или эпителием, сообщающий неизменённый просвет пищевода с просветом трахеи.
Атрезия пищевода является наиболее распространенным вариантом атрезии желудочно-кишечного тракта. [1]
Эпидемиология
Атрезия пищевода — врожденный порок развития верхних отделов желудочно-кишечного тракта, распространенность которого по оценкам во всем мире варьируется от 1 на 2500 до 1 на 4500 рождений. [2] В Соединенных Штатах распространенность оценивается в 2,3 на 10 000 живорождений. [3] Относительная заболеваемость атрезией пищевода увеличивается с возрастом матери. [4], [5], [6]
Причины атрезии пищевода
Этиологией атрезии пищевода с сопутствующим трахеопищеводным свищом или без него является нарушение разделения или неполное развитие передней кишки. [7] Свищевой тракт происходит из ветви эмбрионального зачатка легкого, которая не может разветвляться из-за дефектных эпителиально-мезенхимальных взаимодействий.
С атрезией пищевода связано несколько генов, включая Shh, [8] SOX2, CHD7, MYCN и FANCB. Однако этиология до конца не известна и, вероятно, является многофакторной. У пациентов может быть диагностирован либо изолированный АП/ТПС, либо часть синдрома, такого как VACTERL или CHARGE.
Патогенез
Пищевод представляет собой мышечную трубку, которая транспортирует пищевой комок из глотки в желудок. Пищевод происходит из зародышевого листка энтодермы, который образует глотку, пищевод, желудок и эпителиальные линии аэродигестивного тракта. Трахея и пищевод возникают в результате разделения общей трубки передней кишки на ранних этапах развития плода. [9] Невозможность отделения или полного развития этой общей трубки передней кишки может привести к трахеопищеводному свищу (ТПС) и атрезии пищевода (АП). Пренатально у пациенток с атрезией пищевода может наблюдаться многоводие, преимущественно в третьем триместре, что может быть диагностическим ключом к атрезии пищевода.
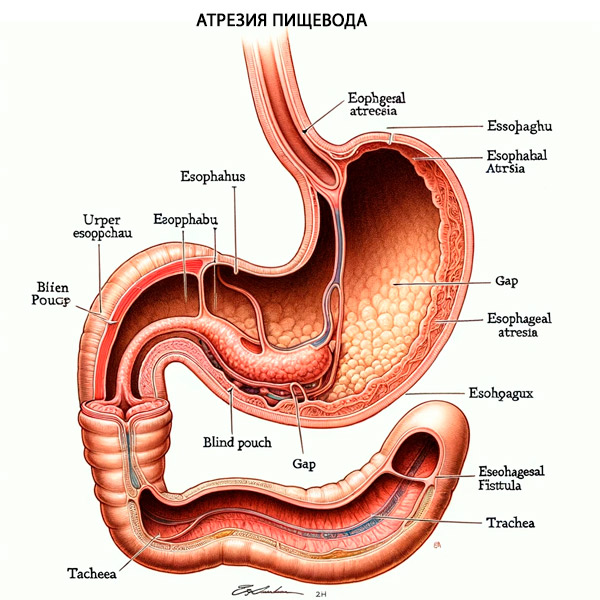
Кроме того, примерно у 50% пациентов с ТПС/АП будут сопутствующие врожденные аномалии, включая VACTERL (дефекты позвонков, анальная атрезия, пороки сердца, трахеопищеводный свищ, почечные аномалии и аномалии конечностей) или CHARGE (колобома, пороки сердца, атрезия хоан, задержка роста)., генитальные аномалии и аномалии ушей). После рождения новорожденного наиболее распространенными симптомами атрезии пищевода являются чрезмерное слюнотечение, удушье и невозможность проведения назогастрального зонда. Кроме того, если имеется сопутствующая ТПС, произойдет газовое растяжение желудка, поскольку воздух проходит из трахеи через дистальный пищеводный свищ, а затем в желудок.
Пациенты с этим комплексом симптомов должны пройти ускоренное обследование на предмет атрезии пищевода и трахеопищеводного свища и незамедлительно направиться на более высокий уровень медицинской помощи для обследования у детского хирурга.
Патофизиология
Трахеопищеводный свищ и атрезия пищевода возникают в результате дефектного латерального разделения передней кишки на пищевод и трахею. Свищевой ход между пищеводом и трахеей, возможно, формируется вторично вследствие дефекта эпителиально-мезенхимальных взаимодействий. [6] Трахеопищеводный свищ и атрезия пищевода присутствуют вместе примерно в 90% случаев. Атрезия пищевода и трахеопищеводный свищ подразделяются на 5 категорий в зависимости от анатомической конфигурации. [10]
- Тип А — изолированная атрезия пищевода без сопутствующего трахеопищеводного свища, распространенность которого составляет 8%.
Проксимальный и дистальный отделы пищевода заканчиваются слепо и не связаны с трахеей. Проксимальный сегмент пищевода расширен, толстостенен и обычно заканчивается выше в заднем средостении, около второго грудного позвонка. Дистальный отдел пищевода короткий и заканчивается на разном расстоянии от диафрагмы. Расстояние между двумя концами будет определять, возможно ли первичное восстановление (редко) или следует выполнить отсроченный первичный анастомоз или замену пищевода. В этих случаях важно исключить проксимальный трахеопищеводный свищ.
- Тип Б — атрезия пищевода с проксимальным трахеопищеводным свищом. Это самый редкий вид, распространенность которого составляет 1%.
Эту редкую аномалию необходимо отличать от изолированной разновидности. Свищ находится не на дистальном конце верхнего мешка, а на 1–2 см выше его конца на передней стенке пищевода.
- Атрезия пищевода типа С является наиболее распространенной (84-86%) и включает проксимальную атрезию пищевода с дистальной трахеопищеводной фистулой.
Это атрезия, при которой проксимальный отдел пищевода расширен, а мышечная стенка утолщена, слепо заканчивается в верхнем средостении примерно на уровне третьего или четвертого грудного позвонка. Дистальный отдел пищевода, который тоньше и уже, входит в заднюю стенку трахеи у киля или, что чаще, на один-два сантиметра проксимальнее трахеи. Расстояние между слепым проксимальным отделом пищевода и дистальным трахеопищеводным свищом варьирует от перекрывающихся сегментов до широкой щели. Очень редко дистальный свищ может быть окклюзирован или облитерирован, что приводит к ошибочному диагнозу изолированной атрезии до операции.
- Тип D — атрезия пищевода с проксимальной и дистальным трахеопищеводным свищом, встречается редко - около 3%
У многих из этих младенцев аномалия была неправильно диагностирована и лечилась как проксимальная атрезия и дистальный свищ. В результате рецидивирующих респираторных инфекций при проведенном обследовании выявлен трахеопищеводный свищ, ранее ошибочно принятый за рецидивирующий свищ. С увеличением использования предоперационной эндоскопии (бронхоскопии и/или эзофагоскопии) «двойной» свищ можно распознать на ранней стадии и выполнить полное восстановление при первоначальной процедуре. Если проксимальный свищ не выявлен до операции, диагноз следует заподозрить по большой утечке газа, исходящей из верхнего мешка во время формирования анастомоза.
- Атрезия пищевода типа Е представляет собой изолированный трахеопищеводный свищ без сопутствующей атрезии пищевода. Он известен как тип «H», его распространенность составляет около 4%.
Между анатомически неповрежденным пищеводом и трахеей имеется свищевое соединение. Свищевой ход может быть очень узким, диаметром 3–5 мм и обычно располагается в нижнешейном отделе. Обычно они одиночные, но описаны два и даже три свища.
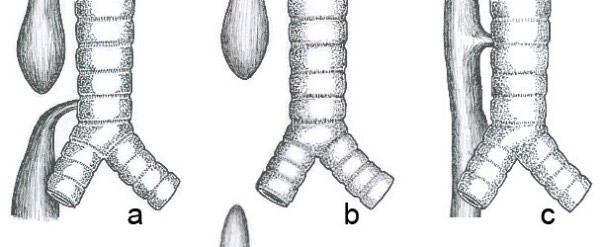
Распространенные анатомические типы атрезии пищевода. а) Атрезия пищевода с дистальным трахеопищеводным свищом (86%). б) Изолированная атрезия пищевода без трахеопищеводного свища (7%). в) трахеопищеводный свищ Н-типа (4%)
Симптомы атрезии пищевода
Примерно у одной трети плодов атрезия пищевода и трахеопищеводный свищ диагностируются пренатально. Наиболее распространенным сонографическим признаком атрезии пищевода является многоводие, которое наблюдается примерно у 60% беременностей. [11] Если диагноз поставлен пренатально, семью можно проконсультировать по поводу ожиданий после родов.
Однако во многих случаях диагноз не диагностируется до рождения. У младенцев с атрезией пищевода симптомы проявляются вскоре после рождения, с увеличением секреции, что приводит к удушью, респираторному дистрессу или эпизодам цианоза во время кормления. При атрезии пищевода свищ между трахеей и дистальным отделом пищевода приводит к заполнению желудка газом на рентгенограмме грудной клетки. У младенцев с атрезией пищевода типа А и В не будет вздутия живота, поскольку нет свища от трахеи до дистального отдела пищевода. Младенцы с трахеопищеводным свищом могут забрасывать содержимое желудка через фистулу в трахею, что приводит к аспирационной пневмонии и респираторному дистрессу. У пациентов с атрезией пищевода типа Е диагноз может быть отложен, если фистула небольшого размера. [12]
Где болит?
Что беспокоит?
Формы
Известно около 100 вариантов этого порока, однако выделяют три наиболее распространенных:
- атрезия пищевода и свищ между дистальной частью пищевода и трахеей (86-90%),
- изолированная атрезия пищевода без свища (4-8%),
- трахеопищеводный свищ, «тип Н» (4%).
В 50-70% случаев атрезии пищевода встречаются сочетанные пороки развития:
- врожденные пороки сердца (20-37%),
- пороки ЖКТ (20-21%),
- дефекты мочеполовой системы (10%),
- дефекты опорно-двигательного аппарата (30%),
- дефекты черепно-лицевой области (4%).
В 5-7% случаев атрезия пищевода сопровождается хромосомными аномалиями (трисомия 18, 13 и 21). Своеобразное сочетание аномалий развития при атрезии пищевода обозначены как «VATER» по начальным латинским буквам следующих пороков развития (5-10%):
- пороки позвоночника (V),
- пороки заднего прохода (А),
- трахеопищеводный свищ (Т),
- атрезия пищевода (Е),
- дефекты лучевой кости (R).
30-40% детей с атрезией пищевода не доношены до срока или имеют задержку внутриутробного развития. [13], [14], [15]
Осложнения и последствия
После восстановления атрезии пищевода могут возникнуть хирургические осложнения. Самым грозным осложнением является несостоятельность пищеводного анастомоза. [16] Небольшие утечки можно устранить с помощью дренирования плевральной дренажной трубки и длительного NPO до тех пор, пока утечка не будет устранена. Если имеется большая несостоятельность или несостоятельность анастомоза, то может потребоваться повторная операция и резекция пищевода с интерпозицией желудочного, толстокишечного или тощекишечного трансплантата.
Другим потенциальным осложнением является стриктура пищеводного анастомоза. Обычно их лечат с помощью серийных эндоскопических расширений пищевода. [17] Наконец, хотя и редко, сообщалось о повторной фистулизации пищевода и трахеи. Эти проблемы лечатся повторной операцией.
Нехирургические осложнения наличия атрезии пищевода и трахеопищеводного свища распространены. Использование ингибиторов протонной помпы рекомендуется в течение как минимум одного года после восстановления атрезии пищевода из-за нарушения моторики пищевода, которое приводит к усилению гастроэзофагеального рефлюкса (ГЭР) и риска аспирации. [18] Трахеомаляция обычно наблюдается после хирургического вмешательства. У новорожденных с атрезией пищевода и трахеопищеводным свищом обычно наблюдается повышенная частота дисфагии, инфекций дыхательных путей и эзофагита. [19]
Из-за повышенного ГЭР в детстве и во взрослом возрасте у этих детей чаще встречается пищевод Барретта и более высокий риск рака пищевода по сравнению с населением в целом. [20] У таких пациентов рекомендуются протоколы скрининга рака пищевода, хотя это противоречиво.
Диагностика атрезии пищевода
Атрезия пищевода обычно диагностируется при невозможности проведения орогастрального зонда. Трубка не доходит до желудка и на рентгенограмме грудной клетки ее можно увидеть свернутой выше уровня атрезии пищевода. Окончательный диагноз можно поставить путем введения небольшого количества водорастворимого контрастного вещества в орогастральный зонд под рентгеноскопическим контролем. Следует избегать применения бария, поскольку он может привести к химическому пневмониту при аспирации в легкие. Для уточнения диагноза можно использовать эзофагоскопию или бронхоскопию для выявления фистулы трахеи. [21]
Новорожденный с атрезией пищевода и трахеопищеводным свищом нуждается в обследовании на наличие аномалий VACTERL и CHARGE, поскольку они могут возникнуть у 50% новорожденных. В частности, для полной оценки требуется эхокардиограмма сердца, рентгенография конечностей и позвоночника, УЗИ почек и тщательный физический осмотр ануса и гениталий на предмет каких-либо отклонений. [22], [23] В крупном одноцентровом исследовании в США были изучены наиболее распространенные врожденные аномалии, связанные с атрезией пищевода и трахеопищеводным свищом. Среди почти 3000 пациентов сопутствующие диагнозы VACTERL включали аномалии позвоночника у 25,5%, аноректальные пороки развития у 11,6%, врожденные пороки сердца у 59,1%, заболевания почек у 21,8% и дефекты конечностей у 7,1%. [24] Почти одна треть имела 3 или более аномалий и соответствовала критериям диагноза VACTERL.
Что нужно обследовать?
Как обследовать?
Дифференциальная диагностика
Дифференциальный диагноз включает расщелины гортани, трахеи и пищевода, перегородки или кольца пищевода, стриктуры пищевода, трубчатые удвоения пищевода, врожденный короткий пищевод и агенезию трахеи. Эти диагнозы можно дополнительно исследовать с помощью различных методов визуализации: от рентгена и компьютерной томографии до эндоскопии и хирургического вмешательства.
К кому обратиться?
Лечение атрезии пищевода
После постановки диагноза атрезии пищевода ребенка следует интубировать, чтобы контролировать проходимость дыхательных путей и предотвратить дальнейшую аспирацию. Если это еще не сделано, следует аккуратно ввести катетер для отсасывания орофарингеальных выделений. Младенцу следует давать антибиотики, внутривенно вводить жидкости и ничего не давать перорально. Для младенца следует рассмотреть возможность полного парентерального питания (ППП). Как только новорожденный стабилизируется с точки зрения гемодинамики и проходимости дыхательных путей, следует проконсультироваться с детским хирургом.
Сроки окончательного хирургического лечения атрезии пищевода зависят от размера новорожденного. Если вес ребенка превышает 2 килограмма, операция обычно предлагается после устранения сердечных аномалий, если таковые имеются. Новорожденных с очень низкой массой тела при рождении (<1500 граммов) обычно лечат поэтапно с первоначальной перевязкой фистулы с последующей пластикой атрезии пищевода, когда новорожденный становится крупнее. [25]
Хирургические варианты восстановления атрезии пищевода включают открытую торакотомию или торакоскопическую хирургию с видеоассистентом. [26] В обеих операциях этапы одинаковы. Выявляют свищ между пищеводом и трахеей и пересекают его. Бронхоскоп можно использовать для визуализации места начала фистулы в трахее. После перевязки свища устраняют атрезию пищевода. Обычно небольшой назогастральный зонд устанавливается так, чтобы пересекать два конца, и концы сшиваются рассасывающейся нитью, если концы достигаются без слишком большого натяжения. Если концы пищевода слишком сильно натянуты или они не достигаются, можно использовать технику Фокера. [27] В этом методе используются швы-тяги на концах пищевода и медленное их сближение. Как только концы сойдутся без натяжения, можно будет выполнить первичный ремонт.
Если имеется сверхдлинный разрыв пищевода, исключающий первичный анастомоз, то можно использовать вставку другого органа, такого как желудок, толстая кишка или тощая кишка. [28] Пациентов с атрезией пищевода типа E «H-типа» можно лечить с помощью высокого разреза шейки матки и избегать торакотомии для перевязки свища. [29] Гастростомия обычно не показана, если первичный анастомоз не оказался неудачным.
После операции новорожденного возвращают в отделение интенсивной терапии новорожденных для тщательного наблюдения. Плевральная дренажная трубка остается на той стороне, к которой осуществлялся доступ к грудной клетке. Новорожденному продолжают полное парентеральное питание с помощью назогастрального зонда с периодическим отсасыванием. Через 5-7 дней проводят эзофагографию для выявления несостоятельности пищевода. Если утечки не обнаружено, обычно начинают пероральное кормление. Если есть утечка, плевральная дренажная трубка соберет дренаж. Плевральную дренажную трубку оставляют на месте до тех пор, пока утечка не закроется и/или новорожденный не перенесет пероральное питание.
Прогноз
Прогноз для новорожденных с атрезией пищевода и трахеопищеводным свищом относительно хороший и зависит главным образом от сердечных и хромосомных аномалий, а не от атрезии пищевода как таковой. Как правило, общая выживаемость составляет около 85–90%. [30] Более высокая смертность наблюдается, когда в дополнение к атрезии пищевода присутствуют сопутствующие сердечные аномалии. Ранние смерти связаны с сердечными аномалиями, тогда как поздние смерти связаны с респираторными осложнениями. Расстояние между двумя пищеводными мешками, особенно если оно большое, может определять прогноз. [31] У всех новорожденных, перенесших восстановление атрезии пищевода, будут ожидаемые желудочно-кишечные и респираторные проблемы, которые обычно улучшаются с возрастом.
Источники
- Nasr T, Mancini P, Rankin SA, Edwards NA, Agricola ZN, Kenny AP, Kinney JL, Daniels K, Vardanyan J, Han L, Trisno SL, Cha SW, Wells JM, Kofron MJ, Zorn AM. Endosome-Mediated Epithelial Remodeling Downstream of Hedgehog-Gli Is Required for Tracheoesophageal Separation. Dev Cell. 2019 Dec 16;51(6):665-674.e6.
- Pretorius DH, Drose JA, Dennis MA, Manchester DK, Manco-Johnson ML. Tracheoesophageal fistula in utero. Twenty-two cases. J Ultrasound Med. 1987 Sep;6(9):509-13.
- Cassina M, Ruol M, Pertile R, Midrio P, Piffer S, Vicenzi V, Saugo M, Stocco CF, Gamba P, Clementi M. Prevalence, characteristics, and survival of children with esophageal atresia: A 32-year population-based study including 1,417,724 consecutive newborns. Birth Defects Res A Clin Mol Teratol. 2016 Jul;106(7):542-8.
- Karnak I, Senocak ME, Hiçsönmez A, Büyükpamukçu N. The diagnosis and treatment of H-type tracheoesophageal fistula. J Pediatr Surg. 1997 Dec;32(12):1670-4.
- Scott DA. Esophageal Atresia / Tracheoesophageal Fistula Overview – RETIRED CHAPTER, FOR HISTORICAL REFERENCE ONLY. In: Adam MP, Feldman J, Mirzaa GM, Pagon RA, Wallace SE, Bean LJH, Gripp KW, Amemiya A, editors. GeneReviews® [Internet]. University of Washington, Seattle; Seattle (WA): Mar 12, 2009.
- Crisera CA, Grau JB, Maldonado TS, Kadison AS, Longaker MT, Gittes GK. Defective epithelial-mesenchymal interactions dictate the organogenesis of tracheoesophageal fistula. Pediatr Surg Int. 2000;16(4):256-61.
- Spitz L. Oesophageal atresia. Orphanet J Rare Dis. 2007 May 11;2:24.
- Lupo PJ, Isenburg JL, Salemi JL, Mai CT, Liberman RF, Canfield MA, Copeland G, Haight S, Harpavat S, Hoyt AT, Moore CA, Nembhard WN, Nguyen HN, Rutkowski RE, Steele A, Alverson CJ, Stallings EB, Kirby RS., and The National Birth Defects Prevention Network. Population-based birth defects data in the United States, 2010-2014: A focus on gastrointestinal defects. Birth Defects Res. 2017 Nov 01;109(18):1504-1514.
- Clark DC. Esophageal atresia and tracheoesophageal fistula. Am Fam Physician. 1999 Feb 15;59(4):910-6, 919-20.
- Lautz TB, Mandelia A, Radhakrishnan J. VACTERL associations in children undergoing surgery for esophageal atresia and anorectal malformations: Implications for pediatric surgeons. J Pediatr Surg. 2015 Aug;50(8):1245-50.
- Petrosyan M, Estrada J, Hunter C, Woo R, Stein J, Ford HR, Anselmo DM. Esophageal atresia/tracheoesophageal fistula in very low-birth-weight neonates: improved outcomes with staged repair. J Pediatr Surg. 2009 Dec;44(12):2278-81.
- Patkowsk D, Rysiakiewicz K, Jaworski W, Zielinska M, Siejka G, Konsur K, Czernik J. Thoracoscopic repair of tracheoesophageal fistula and esophageal atresia. J Laparoendosc Adv Surg Tech A. 2009 Apr;19 Suppl 1:S19-22.
- Foker JE, Linden BC, Boyle EM, Marquardt C. Development of a true primary repair for the full spectrum of esophageal atresia. Ann Surg. 1997 Oct;226(4):533-41; discussion 541-3.
- Bairdain S, Foker JE, Smithers CJ, Hamilton TE, Labow BI, Baird CW, Taghinia AH, Feins N, Manfredi M, Jennings RW. Jejunal Interposition after Failed Esophageal Atresia Repair. J Am Coll Surg. 2016 Jun;222(6):1001-8.
- Ko BA, Frederic R, DiTirro PA, Glatleider PA, Applebaum H. Simplified access for division of the low cervical/high thoracic H-type tracheoesophageal fistula. J Pediatr Surg. 2000 Nov;35(11):1621-2. [PubMed]
- 16.
- Choudhury SR, Ashcraft KW, Sharp RJ, Murphy JP, Snyder CL, Sigalet DL. Survival of patients with esophageal atresia: influence of birth weight, cardiac anomaly, and late respiratory complications. J Pediatr Surg. 1999 Jan;34(1):70-3; discussion 74.
- Upadhyaya VD, Gangopadhyaya AN, Gupta DK, Sharma SP, Kumar V, Pandey A, Upadhyaya AD. Prognosis of congenital tracheoesophageal fistula with esophageal atresia on the basis of gap length. Pediatr Surg Int. 2007 Aug;23(8):767-71.
- Engum SA, Grosfeld JL, West KW, Rescorla FJ, Scherer LR. Analysis of morbidity and mortality in 227 cases of esophageal atresia and/or tracheoesophageal fistula over two decades. Arch Surg. 1995 May;130(5):502-8; discussion 508-9.
- Antoniou D, Soutis M, Christopoulos-Geroulanos G. Anastomotic strictures following esophageal atresia repair: a 20-year experience with endoscopic balloon dilatation. J Pediatr Gastroenterol Nutr. 2010 Oct;51(4):464-7.
- Krishnan U, Mousa H, Dall'Oglio L, Homaira N, Rosen R, Faure C, Gottrand F. ESPGHAN-NASPGHAN Guidelines for the Evaluation and Treatment of Gastrointestinal and Nutritional Complications in Children With Esophageal Atresia-Tracheoesophageal Fistula. J Pediatr Gastroenterol Nutr. 2016 Nov;63(5):550-570.
- Connor MJ, Springford LR, Kapetanakis VV, Giuliani S. Esophageal atresia and transitional care--step 1: a systematic review and meta-analysis of the literature to define the prevalence of chronic long-term problems. Am J Surg. 2015 Apr;209(4):747-59.
- Jayasekera CS, Desmond PV, Holmes JA, Kitson M, Taylor AC. Cluster of 4 cases of esophageal squamous cell cancer developing in adults with surgically corrected esophageal atresia--time for screening to start. J Pediatr Surg. 2012 Apr;47(4):646-51.

