Медицинский эксперт статьи
Новые публикации
Роль изменений в субхондральной кости в патогенезе остеоартроза
Последняя редакция: 19.10.2021

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
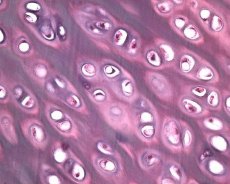
Наряду с дегенерацией суставного хряща, в патологический процесс при остеоартрозе вовлекается и подлежащая костная ткань. Предполагают, что утолщение субхондральной пластинки способствует прогрессированию остеоартроза. По мере прогрессирования остеоартроза суставной хрящ, который является объектом для механического и химического стрессов, медленно эрозируется благодаря дисбалансу процессов катаболизма и репарации хряща. В частности, механический стресс в отношении «несущих» массу тела суставов способствует образованию большого количества микропереломов в субхондральной пластинке и хряще. По мере эрозирования суставного хряща прогрессирует склероз субхондральной кости, повышается жесткость костной ткани, которая в свою очередь способствует дальнейшему нарушению структуры суставного хряща. Однако вопрос о первичности или вторичности изменений субхондральной кости при остеоартрозае остается нерешенным.
До недавнего времени считали, что определяемые рентгенологически изменения в губчатом веществе субхондральной кости, такие, как склероз или образование кист, у больных остеоартроз носят вторичный характер. Однако результаты клинических и экспериментальных исследований свидетельствуют о возможной инициирующей роли субхондральной кости в патогенезе остеоартроза. Одним из возможных механизмов является резкое повышение градиента жесткости субхондральной кости в связи с тем, что целостность надлежащей хрящевой ткани зависит от механических свойств ее костного «ложа». Исследования у приматов показали, что изменения в субхондральной кости могут предшествовать изменениям в суставном хряще. Появившиеся в результате проведенных исследований на моделях остеоартроз у животных и клинических исследований свидетельства в пользу этой гипотезы и против нее только обострили дискуссию. Утолщение трабекул в субхондральной кости не всегда сопровождается повышением минерализации костной ткани, а вернее, увеличением объема остеоида. Этот признак аномальной минерализации свидетельствует о том, что нарушение регуляции ремоделирования костной ткани является неотъемлемой частью остеоартроза, а также свидетельствует в пользу концепции о дефекте клеток костной ткани при остеоартрозе. Группа J. Dequeker (1989) рассматривают последний как «генерализованную метаболическую болезнь костной ткани».
Костная ткань постоянно обновляется. Этот динамичный процесс, который называется ремоделированием костной ткани, представляет собой сложную последовательность процессов резорбции и минерализации. Остеокласты резорбируют костную ткань, а остеобласты секретируют белки, формирующие основной органический компонент для минерализации. Образование и резорбция кости неслучайно происходят по всему скелету, это - запрограммированный процесс, происходящий в различных участках скелета, называемый единицами костного ремоделирования. В начале цикла остеокласты появляются на неактивной поверхности; в течение 2 нед они образуют туннель в кортикальном слое кости или лакуну на поверхности трабекулярной кости. Частота активации новых единиц костного ремоделирования определяет степень обновления костной ткани. У здорового молодого человека процессы формирования и резорбции костной ткани уравновешены, поддерживается нормальная масса костной ткани. В гормональной регуляции резорбции костной ткани, по крайней мере ПТГ и ПГЕ2, принимают участие не только остеокласты, но и остеобласты, так как под действием этих гормонов высвобождаются факторы, стимулирующие резорбцию кости остеокластами. В настоящее время известно более 12 локальных и системных регуляторов роста костной ткани, влияющих на ее ремоделирование, в частности ПТГ, 1,25(OH)2D3, кальцитонин, гормон роста, глюкокортикоиды, гормоны щитовидной железы, инсулин, ИФР (1 и 2), эстрогены, ПГЕ2, андрогены.
Костные клетки высвобождают ряд белков и цитокинов, которые осуществляют эндокринную регуляцию и передачу сигнала. Вырабатываемые остеобластами белки включают белки костного матрикса, такие, как коллаген, остеопонтин, остеокальцин, костные сиалопротеины. Кроме того, эти клетки высвобождают протеазы как в активной, так и в латентной форме, которые принимают участие в процесее ремоделирования костной ткани - ММП, компоненты системы активатор плазминогена (АП)/плазмин. Высвобождаемые остеобластами цитокины могут действовать как посредством аутокринных механизмов, так и паракринным путем на местные клетки (другие остеобласты, остеокласты).
Пока неизвестно, каким путем регулируются эти сигналы - механическим стрессом или другими химическими сигналами, индуцированными механическим стрессом. Однако известно, что повторяющийся механический стресс вызывает локальную пролиферацию костных клеток и/или белков. В условиях in vivo механическая нагрузка способна активировать остеобласты, повышать уровень циклических нуклеотидов, продукцию простагландинов, а также вызывать морфологические изменения, ассоциированные с ремоделированием костной ткани. В условиях in vitro механический стресс вызывает пролиферацию культуры остеобластов, экспрессию мРНК костных белков, принимающих участие в образовании остеоида и в процессе минерализации, высвобождение локальных факторов роста, таких, как ИФР-1 и ИФР-2 и молекул адгезии. Передача сигнала механического стресса может осуществляться посредством механочувствительных ионных каналов.
Существуют косвенные доказательства нарушения функции остеобластов при остеоартрозе. G. Gevers и J. Dequeker (1987) продемонстрировали повышение уровня сывороточного остеокальцина у женщин с остеоартрозом суставов кистей, а также в эксплантатах кортикальной зоны кости, что свидетельствует о том, что патология костной ткани может выступать частью остеоартроза. При аутопсии обнаружено не только утолщение субхондральной кости, но и аномально низкую минерализацию головки бедренной кости. У морских свинок с хирургически индуцированным остеоартрозом с помощью компьютерной томографии обнаружено значительное утолщение костной фракции в субхондральной зоне. Дисбаланс между коллагеновыми и неколлагеновыми (остеокальцин и др.) белками может привести к увеличению объема костной ткани, но не влияет на ее минеральную плотность. По данным М. Shimizu и соавторов (1993), прогрессирование дегенеративных изменений суставного хряща ассоциируется с более интенсивным ремоделированием субхондральной кости и повышением ее жесткости, что также указывает на дефект клеток костной ткани при остеоартрозе. Согласно предложенной В. Lee и М. Aspden (1997) гипотезе, пролиферация дефектных костных клеток может привести к повышению жесткости костной ткани, но не вызывает повышения ее минеральной плотности.
C.I. Westacott и соавторы (1997) выдвинули гипотезу о том, что аномальные остеобласты непосредственно влияют на метаболизм хрящевой ткани. Культивируя остеобласты пациентов с остеоартрозом с хондроцитами людей, у которых не было болезней суставов, авторы наблюдали значительное изменение высвобождения гликозаминогликанов нормальной хрящевой тканью in vitro, однако уровень высвобождения цитокинов оставался неизмененным. G. Hilal и соавторы (1998) показали, что культура остеобластов субхондральной кости больных с остеоартрозом in vitro имеет измененный метаболизм - активность системы АП/плазмин и уровень ИФР-1 в этих клетках повышены. Наблюдение C.I. Westacott и соавторов (1997) можно объяснить повышением активности протеаз клетками субхондральной кости.
Остается неизвестным, инициируют ли остеоартроз изменения в субхондральной кости или способствуют его прогрессированию? D.K. Dedrick и соавторы (1993) продемонстрировали, что у собак с хирургически индуцированным остеоартрозом утолщение субхондральной кости не является необходимым условием для развития остеоартрозподобных изменений суставного хряща, однако способствует прогрессированию дегенеративных процессов в хряще. Результаты исследования A. Sa'ied и соавторов (1997) противоречат данным предыдущего исследования. Используя 50 МГц эхографию для оценки начальных морфологических изменений и их прогрессирования в суставном хряще и кости при экспериментальном остеоартрозе, индуцированном инъекциями монойодуксусной кислоты в коленный сустав крыс, авторы продемонстрировали одновременный процесс изменений в кости и хряще в течение первых трех дней после инъекции.
Остеобласты секретируют факторы роста и цитокины, принимающие участие в локальном ремоделировании костной ткани, что может способствовать ремоделированию надлежащей хрящевой ткани в «несущих массу тела» суставах после их проникновения через микротрещины в кальцифицированном слое суставного хряща. Более того, продукты секреции костных клеток обнаруживают в синовиальной жидкости. Наиболее вероятными продуктами, выделяемыми аномальными остеобластами, способными запускать процесс локального ремоделирования хрящевой ткани, являются ТФР-b и костные морфометрические протеины (КМП). Оба представителя семейства ТФР выделяются и хондроцитами и остеобластами и оба способны модифицировать ремоделирование как костной, так и хрящевой ткани. J. Martel Pelletier и соавторы (1997) наблюдали повышение уровня ТФР-Р в эксплантатах субхондральной кости больных остеоартрозом по сравнению со здоровыми людьми, что свидетельствует о вероятной роли этого фактора роста в патогенезе остеоартроза. ИФР также продуцируются остеобластами. В культуре остеобластоподобных клеток, полученных от больных с остеоартрозом, обнаружено повышение уровня ИФР, которые изменяют метаболизм хряща.
ТФР-b, ИФР, КМП и цитокины, продуцируемые остеобластами в субхондральной кости, могут влиять на продукцию коллагеназы и других протеолитических ферментов в хряще, что в свою очередь, может способствовать ремоделированию/деградации хрящевого матрикса. Остается неясным, вырабатывают ли остеобласты при ОА меньше макрофагального колониестимулирующего фактора (М-КСФ - стимулятор костной резорбции), чем нормальные клетки. Результаты исследований A. G. Uitterlinden и соавторов (1997) показали, что определенную роль в образовании остеофитов могут играть рецепторы витамина D, которые экспрессируются остеобластами и регулируют экспрессию ряда факторов, синтезируемых этими клетками, что частично объясняет роль остеобластов в патогенезе этого заболевания.
Учитывая результаты вышеприведенных исследований, G. Hilal и соавторы (1998), J. Martel-Pelletier и соавторы (1997) предложили следующую рабочую гипотезу взаимоотношений ремоделирования субхондральной кости и надлежащего суставного хряща при остеоартрозе. На ранней или развернутой стадии патогенеза ОА интенсифицируется процесс ремоделирования костной ткани в субхондральной кости. Одновременно повторяющаяся нагрузка ведет к локальным микропереломам и/или появлению дисбаланса системы ИФР/ИФР-связываюший белок (ИФРСБ) вследствие аномального ответа остеобластов субхондральной кости, что способствует ее склерозу. Последнее в свою очередь может способствовать появлению микропереломов надлежащего хряща и повреждению его матрикса.
В нормальных условиях это повреждение устраняется путем локального синтеза и высвобождения ИФР-1 и ИФР-связывающего белка, которые стимулируют образование ВКМ суставного хряща. В то же время ФР-система способствует росту клеток субхондральной кости и формированию костного матрикса. Анаболическая активность ИФР-системы повышена в субхондральной кости больных остеоартрозом, тогда как локальная активация системы АП/плазмин (местный регулятор ИФР-системы) в суставном хряще обусловливает его локальные изменения. В остеобластах при остеоартрозе ИФР-1 нарушает регуляцию АП плазмином по типу положительной обратной связи, следовательно, может сдерживать ремоделирование в костной ткани, что в итоге приводит к субхондральному склерозу. Таким образом, в костной и хрящевой ткани локальная индукция ИФР-1 ипротеаз ведет, с одной стороны, к повреждению хряща, с другой - к утолщению субхондральной кости, последнее в свою очередь способствует дальнейшему повреждению хряща. Дисбаланс между повреждением хряща, связанным с субхондральным склерозом, и его репаративными способностями ведет к прогрессирующему изменению ВКМ хряща и к развитию остеоартроза. По мнению авторов, эта гипотеза также объясняет медленное прогрессирование болезни.

