Медицинский эксперт статьи
Новые публикации
Диагностика стадий течения рака предстательной железы
Последняя редакция: 23.11.2021

Весь контент Web2Health проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Клинически различают локализованный T1-2, N0, M0), местнораспространённый (Т3-4, N0-1, M0) и генерализованный рак (T1-4, N0-1, М1).
Больных с клинически локализованными и местнораспространёнными стадиями распределяют по степени риска (Д’Амико А В. и др., 2003):
- низкая: стадия Т1а-с; уровень ПСА менее 10 иг/мл: градация по Глисону - 2-5; при биопсии - одностороннее поражение менее 50%:
- умеренная: стадия Т2а; уровень ПСА менее 10 нг/мл; градация по Глисону - 3 + 4 = 7; при биопсии - двустороннее поражение менее 50%;
- высокая стадия Т2b , Т3а-b; уровень ПСА - 10-20 нг/мл; градация по Глисону - более 4 + 3 - 7; при биопсии - поражение более 50%, периневральная инвазия;
- очень высокая: стадия Т4; уровень ПСА более 20 нг/мл; градация по Глисону - более 8; при биопсии - лимфоваскулярная инвазия.
После уточнения диагноза и установления распространённости процесса (локализованный, местнораспространенный или генерализованный) врач и пациент стоят перед выбором метода лечения. В современном обществе огромное значение уделяют качеству жизни больных после начала лечения. Качество жизни без лечения соответствует течению основного заболевания и зависит от прогрессирования онкологического процесса. Изменение качества жизни возникает в основном после начала лечения и применения одного из терапевтических или хирургических методов. Чёткое установление стадии процесса позволяет не только выбрать оптимальный метод лечения, но и прогнозировать дальнейшее течение заболевания.
Определение уровня ПСА в сочетании с клинической картиной рака простаты и градацией опухоли по шкале Глисона значительно повышает информативность каждого из перечисленных показателей в установлении патологической стадии рака. А.В. Партин и соавт. (1997) предложили прогностические таблицы, позволяющие прогнозировать дальнейшее распространение опухоли, выбор метода лечения, степень радикальности и прогноз эффективности лечения
Для оценки распространённости опухоли наиболее часто используют ПРИ, ТРУЗИ, определение уровня ПСА и остеосцинтиграфию. При необходимости назначают компьютерную томографию (КТ) или магнитно-резонансную томографию (MPТ) и рентгенографию грудной клетки.
Любой из методов визуализации предназначен для определения стадии и оценки эффективности лечения После верификации диагноза уролог должен уточнить объём первичной опухоли, ее границы, инвазивный или метастатический потенциал опухоли. Все эти показатели имеют большое значение для прогноза заболевания и выбора метода лечения.
Первичная опухоль (Т)
Прежде всего, следует определить, ограничена опухоль предстательной железой (Т1-2) или выходит за пределы капсулы (Т3-4). Пальцевое исследование часто не позволяет оценить распространённость опухоли. По некоторым данным, результаты ПРИ соответствуют таковым при гистологическом исследовании менее чем у 50% больных. Тем не менее более подробное обследование показано лишь при решении вопроса о радикальном лечении.
Уровень ПСА может отражать распространённость опухоли, однако не позволяет точно определить морфологическую стадию. Сочетание уровня ПСА, индекса Глисона и данных пальпации позволяет лучше предсказать морфологическую стадию, чем каждый из этих параметров в отдельности. Значение свободного ПСА спорно: в одном из исследований определение содержания свободного ПСА помогало уточнить стадию при локализованных опухолях, однако другие работы этого не подтвердили. Разрешить этот вопрос помогут лишь углублённые исследования.
Для изучения состояния предстательной железы чаще всего применяют трансректальное УЗИ. Этот метод позволяет обнаружить лишь 60% опухолей и не всегда показывает прорастание капсулы. Почти у 60% больных со стадией Т3. УЗИ указывает на менее распространённый процесс. Ультразвуковые признаки прорастания капсулы - выпуклость, неровность и разрыв контура железы. Инвазия опухолевых клеток в семенные пузырьки - плохой прогностический признак, но информация о ней крайне важна для выбора метода лечения. При ТРУЗИ следует обращать внимание на эхоструктуру пузырьков (гиперэхогенность), их асимметрию, деформацию и расширение. Также о поражении семенных пузырьков свидетельствует утрата закругленности и уплотнение у основания железы. Эти признаки довольно субъективны, поэтому целиком полагаться на данные УЗИ нецелесообразно. Инвазия семенных пузырьков указывает на высокий риск местного рецидива и метастазов и для уточнения (перед операций) показана их биопсия. Начинать обследование с этой процедуры не следует, но если риск инвазии велик и от результата биопсии зависит выбор лечения, то её выполнение оправданно. Отрицательный результат не исключает микроскопической инвазии. Как правило, биопсию семенных пузырьков проводят при клинической стадии Т2b, и выше и содержании ПСА более 10 нг/мл. Результат считают положительным, если хотя бы один биоптат из основания предстательной железы содержит опухолевые клетки. Повысить точность клинического определения стадии позволяют не только дополнительные исследования, но и тщательный анализ результатов первичной биопсии (играют роль количество и протяжённость опухолевых очагов, инвазия капсулы). Имеет значение и степень дифференцировки: при индексе Глисона менее 6 опухоль в 70% случаев локализована.
Кровоток в предстательной железе при раке выше, чем в нормальной железе или при ее гиперплазии. После кастрации интенсивность кровотока в железе снижена. Перспективна разработка эходопплерографических карт для диагностики и мониторинга РПЖ, однако в настоящее время нет достоверных данных об использовании эходопплерографии в определении стадии местного процесса. Возможно применение этого метода для получения дополнительного материала при прицельной биопсии из очагов патологической васкуляризации.
Результаты визуализации рака простаты прямо зависят от технической оснащённости клиники и опыта специалиста. Именно поэтому все современные методы визуализации носят не определяющую, а уточняющую роль, и выбор метода лечения основан на совокупности данных клинического обследования и инструментальных исследований.
Наилучшими возможностями для визуализации структуры предстательной железы обладает МРТ. Современный стандарт обследования органов малого таза методом MPТ - применение эндоректального датчика, позволяющего получить изображение с максимально возможным пространственным разрешением, составляющим 0,5-1 мм. Нагнетание воздуха в эндоректальный датчик обеспечивает чёткую визуализацию капсулы предстательной железы, ректопростатических углов и ректопростатической фасции Денонвилье. Применение эндоректального датчика при MРТ не ограничивает визуализацию регионарных лимфатических узлов (вплоть до уровня бифуркации брюшной аорты). Раку предстательной железы свойственна низкая интенсивность сигнала на Т-взвешенных изображениях на фоне сигнала высокой интенсивности от неизмененной периферической зоны железы. Неправильная форма, диффузное распространение с масс-эффектом, нечёткие и неровные контуры - морфологические характеристики очагов низкой интенсивности сигнала в периферической зоне предстательной железы, позволяющие предположить неопластический характер поражения. При проведении динамического контрастирования очаги рака быстро накапливают контрастный препарат в артериальную фазу и быстро выводят препарат, что отражает степень ангиогенеза и, соответственно, степень злокачественности опухоли. Низкая интенсивность сигнала также свойственна очагам постбиопсийных кровоизлияний, простатита, стромальной доброкачественной гиперплазии нейтральной зоны железы, фиброзно-рубцовым изменениям, фибромускулярной гиперплазии, последствиям гормональной или лучевой терапии. МРТ без динамического контрастирования не позволяет достоверно дифференцировать большинство перечисленных изменений и заболеваний.
Как отмечено выше, одна из основных задач любого метода визуализации при РПЖ - определение объёма поражения железы и распространения опухоли за пределы капсулы. Определение объема опухоли важно в прогностическом отношении. Объём опухоли менее 4 см3 свидетельствует об отдалённых метастазах, а 12 см3 - о крайне высокой вероятности метастазов. По данным исследований, точность МРТ в обнаружении очагов неопластического поражения предстательной железы составляет от 50 до 90%. Чувствительность МРТ при определении локализации РПЖ составляет около 70-80%, при этом микроскопические очаги рака (фокусы) с помощью МРТ обнаружить невозможно.
Важнейшее преимущество эндоректальной MPТ - возможность определения локализации очагов неопластического поражения в зонах, недоступных другим методам диагностики, и уточнения характера и направления роста опухоли. Так, например, МРТ позволяет обнаружить очаги неопластического поражения в передних отделах периферической зоны предстательной железы, недоступных при трансректальной биопсии. В целом МРТ существенно дополняет данные ПРИ и ТРУЗИ о локализации опухоли.
Эндоректальная MPТ позволяет визуализировать капсулу железы, сосудисто-нервные пучки, семенные пузырьки, верхушку железы, перипростатичсское венозное сплетение и определить локальную распространённость опухоли железы. Следует подчеркнуть, что пенетрацию капсулы считают микроскопическим признаком, и даже современные аппараты МРТ (эндоректальная катушка) не способны дать такую информацию. Возможно лишь получение данных о прорастании за пределы капсулы железы.
Критерии диагностики экстракапсулярной экстензии при МРТ:
- наличие собственно экстракапсулярной опухоли;
- неровность контура железы (деформация, ангулярность);
- асимметрия нейроваскулярных пучков;
- облитерация ректопростатических углов;
- широкий контакт опухоли с капсулой.
Самой высокой специфичности (до 95-98%) и точности результата МРТ достигают при обследовании пациентов среднего или высокого риска экстракапсулярной инвазии. Считают, что экстракапсулярная инвазия (по данным МРТ) указывает на нецелесообразность хирургического лечения и неблагоприятный прогноз заболевания. Гормональная или лучевая терапия не влияет на точность обнаружения экстракапсулярного распространения опухоли предстательной железы. Основная трудность в обнаружении очагов рака и экстракапсулярного распространения опухоли - высокая вариабельность интерпретации томограмм разными специалистами. Первостепенная задача специалиста по лучевой диагностике - достижение высокой специфичности диагностики (даже в ущерб чувствительности) для того, чтобы не лишить операбельных пациентов шанса на проведение радикального лечения.
Сходство плотности раковой, гиперплазированной и нормальной ткани предстательной железы при КТ делает этот метод малопригодным для оценки местной распространенности опухоли. Прорастание в семенные пузырьки более важно, чем прорастание в капсулы, но и в этом случае КТ даёт информацию лишь при запущенном процессе. Однако этот метод активно применяют для разметки области воздействия перед лучевой терапией.
Медленное развитие лучевой диагностики в нашей стране привело к поздней диагностике РПЖ и, следовательно, к недостаточной распространённости радикальных методов лечения РПЖ (например, простатэктомии), малой доступности современных томографов и отсутствию соответствующих обучающих программ для специалистов по лучевой диагностике и урологов. Несмотря на то что КТ и МРТ сейчас широко распространены, уровень оснащения кабинетов и образования специалистов по лучевой диагностике недостаточен для того, чтобы полученная информация стала определяющей при выборе метода лечения больных РПЖ.
Регионарные лимфатические узлы (N)
Оценивать регионарные лимфатические узлы следует лишь в тех случаях, когда это напрямую влияет на лечебную тактику (обычно при планировании радикального лечения). Высокий уровень ПСА, опухоли Т2с-Т3а, низкая дифференцировка и периневральная инвазия сопряжены с высоким риском метастазирования в лимфатические узлы. Оценку состояния лимфатических узлов по уровню ПСА считают недостаточной.
Необходимую информацию предоставляет лишь лимфаденэктомия (открытая или лапароскопическая). Недавние исследования расширенной лимфаденэктомии показали, что РПЖ не всегда поражает запирательные лимфатические узлы. При бессимптомных опухолях и уровне ПСА менее 20 кг/мл. КТ подтверждает увеличение лимфатических узлов лишь в 1 % случаев. Применение МРТ или КТ оправдано при высоком риске метастазирования, так как специфичность этих методов достигает 93-96%. Однако даже положительный результат при их применении может быть ложным, и только пункция подозрительного лимфатического узла позволяет отказаться от лимфаденэктомии, По данным ретроспективного анализа, размеры лимфатического узла не всегда свидетельствуют о наличии в нем метастазов, более информативным признаком считают асимметрию пораженных лимфатических узлов. В настоящее время только у 2-3% больных, перенёсших радикальную простатэктомию по поводу локального РПЖ, диагностируют метастазирование в лимфатические узлы на основании послеоперационного гистологического исследования.
В качестве методов обнаружения метастазирования в лимфатические узлы рекомендуют использовать позитронно-эмиссионную томографию (ПЭТ) и сцинтиграфию с мечеными антителами, но их применение пока ограничено в связи с недостаточной чувствительностью.
Для оценки риска поражения регионарных лимфатических узлов можно использовать номограммы Партина (2001). Номограммы - Математические алгоритмы, которые используют для конкретного пациента или для группы больных. Эти таблицы позволяют определить вероятность местного распространения опухоли (на капсулу, семенные пузырьки) и поражения лимфатических узлов на основании клинической стадии, уровня ПСА и индекса Глисона. В частности, они дают возможность выделить группу больных с низкой (менее 10%) вероятностью метастазирования в лимфатические узлы (при уровне ПСА более 20 нг/мд, стадии Т1-2а и индексе Глисона 2-6); в этой группе перед радикальным лечением состояние лимфатических узлов можно не уточнять. Оценить риск метастазировани я в лимфатические узлы позволяет и обнаружение участков опухоли с выраженной анаплазией (4-5 баллов): если такие участки обнаруживают в четырёх биоптатах и более или они преобладают хотя бы в одном биоптате, риск достигает 20-45%. У остальных больных он не превышает 2,5%. Дополнительное обследование в таких случаях не требуется
Отдалённые метастазы (М)
У 85% больных, умирающих от РПЖ, обнаруживают поражения осевого скелета. Костные метастазы возникают вследствие попадания раковых клеток с током крови в костный мозг, что приводит к росту опухоли и лизису костных структур. Распространенность костных метастазов влияет на прогноз, а их раннее обнаружение предупреждает врача о возможных осложнениях. В 70% случаев метастазирование сочетается с повышением активности костного изофермента щелочной фосфатазы (ЩФ). Определение активности ЩФ и уровня ПСА в подавляющем большинстве случаев позволяет обнаружить костное метастазирование. Поданным многофакторного анализа, на эти показатели влияет лишь количество метастазов в кости. Важно, что активность костного изофермента ЩФ отражает степень поражения костей более точно, чем уровень ПСА.
Наиболее чувствительным методом обнаружения метастазов в кости считают сцинтиграфию (превосходит рентгенографию и определение активности щелочной и кислой фосфатазы). В качестве радиофармацевтического препарата лучше использовать дифосфонаты технеция, накопление которых в костях происходит намного активнее, чем в мягких тканях. Показана корреляция между полуколичественной оценкой поражения костей и выживаемостью. Обнаружение отдалённых метастазов возможно в любом органе. Чаще они возникают в нерегионарных лимфатических узлах, легких, печени, головном мозге и коже. При соответствующих жалобах и симптомах для их обнаружения используют рентгенографию грудной клетки, УЗИ, КТ и МРТ. Тактика при подозрении на костное метастазирование представлена на схеме.
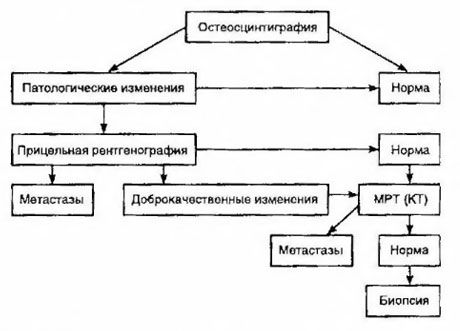
Самым надёжным лабораторным показателем, помогающим в определении степени метастазирования, служит уровень ПСА. Показано, что его увеличение свыше 100 нг/мл - единственный параметр, достоверно указывающий на отдалённые метастазы. Определение уровня ПСА уменьшает число больных, нуждающихся в сцинтиграфии костей. Вероятность обнаружения метастазов в кости при уменьшении уровня ПСА очень низка. При отсутствии жалоб и исходном содержании ПСА менее 20 нг/мл, обнаружении высоко- и умереннодифференцированных опухолей от сцинтиграфии можно отказаться. В то же время при низкодифференцированных опухолях и прорастании капсулы показана сцинтиграфия (независимо от уровня ПСА).


 [
[